La clinique la plus récompensée
Rencontrez ici nos prix d’excellence et de recherche. Découvrez nos taux de réussite.
Découvrez nos installations à Barcelone, notre philosophie, nos valeurs et nos projets
Programme pour l’attribution des donneurs selon les traits héréditaires de votre personnalité
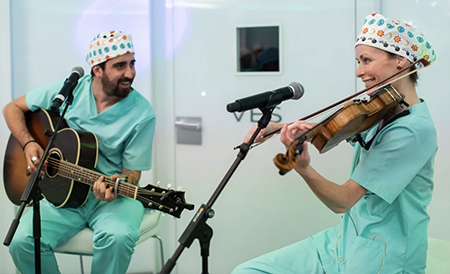
La musique améliore la Fécondation In Vitro
Dans nos laboratoires, nous organisons des concerts en direct pour nos embryons avec de grandes stars de la musique. Antonio Orozco, Alex Ubago, Sharon Corr et Hugo Marlo sont quelques-uns des artistes qui se sont produits exclusivement pour nos petits patients, dans le but de favoriser leur développement embryonnaire.
Que pouvez-vous faire pour améliorer vos chances d’implantation d’embryons?
Observez vos embryons sur votre portable avec l’Embryomobile: Institut Marquès est un centre d’excellence et de transparence en matière de procréation médicalement assistée car c’est le seul centre où vous pouvez vraiment voir l’état de vos embryons.
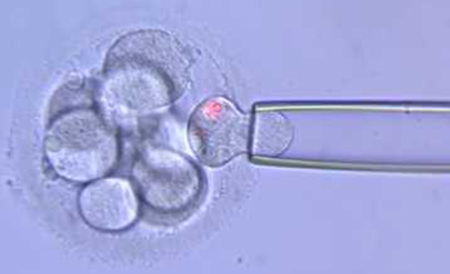
Test génétique préimplantatoire EXPRESS
Très peu de centres ont la possibilité d’offrir à leurs patients l’étude génétique de leurs embryons dans les 48 heures. Avec le traitement de FIV par PGT Express, l’Institut Marquès propose la biopsie et l’analyse de tous les chromosomes lorsque l’embryon est âgé de trois jours.

« Nous créons des familles dans plus de 50 pays »
Transparence et sécurité : nous sommes le seul centre où vous pouvez voir les résultats de votre cycle en direct.
Découvrez ici votre réserve ovarienne grâce à quelques tableaux élaborés par l’Institut Marquès.
Comment sélectionnons-nous nos donneurs ? Puis-je choisir entre donneurs anonymes et non anonymes ?

L’avis du Dr. Marisa López-Teijón
La directrice de l’Institut Marquès a été nommé « Médecin de l’année en Procréation Médicalement Assistée 2019 »
Rajeunissement ovarien
En cas de grossesse tardive, de nombreuses femmes ont besoin d’une Fécondation In Vitro avec don d’ovules. C’est souvent difficile à accepter pour eux. De nombreuses femmes ne l’acceptent pas et veulent faire tout leur possible pour essayer avec leurs propres ovules. Malheureusement, cela conduit à l’émergence de techniques expérimentales, coûteuses, inefficaces et trompeuses.
Lire plus.
L’observation des embryons pendant leur développement grâce à l’Embryomobile augmente les chances de grossesse dans le cadre d’un traitement de Fécondation In Vitro. Savoir plus
Grâce à vous et aux donneurs, notre famille est complète avec trois merveilleux enfants, heureux et en bonne santé. Nous vous sommes tellement reconnaissants et il est aujourd’hui impossible d’imaginer la vie sans ces merveilleux cadeaux.. Savoir plus.